فرق اتانول با متانول
اتانول و متانول هر دو نوع الکل هستند، اما ساختار و خواص شیمیایی متفاوتی دارند که منجر به تفاوت های قابل توجهی در کاربرد، اثرات بر سلامت انسان و کاربردهای صنعتی می شود. در اینجا تفاوت های کلیدی بین اتانول و متانول توضیح داده شده است:

جهت آشنایی با فرق اتانول با متانول (الکل صنعتی) بهتر است ابتدا با این دو الکل بیشتر آشنا شویم اتانول یک الکل ساده با فرمول شیمیایی ch3ch2oh است که به صورت یک مایع فرار قابل اشتعال و بی رنگ ظاهر می شود که دارای بوی مشخص الکلی است
اتانول به طور طبیعی با تخمیر قندها توسط مخمرها یا از طریق فرآیندهای پتروشیمی مانند هیدراتاسیون اتیلن تولید می شود.
این دو ماده با اینکه هر دو الکل های گروه اول می باشند اما با یکدیگر از نظر فرایند تولید، کاربرد و میزان سمی بودن و یا نبودن تفاوت های عمده ای دارند. با توجه به مسمومیت های گزارش شده در اثر مصرف متانول ، بر آن شدیم که در این مقاله درباره ی تفاوت های میان این دو ماده و راه های تشخیص آن ها از یکدیگر بیشتر بپردازیم. پس با ما همراه باشید.
ساختار شیمیایی اتانول و متانول
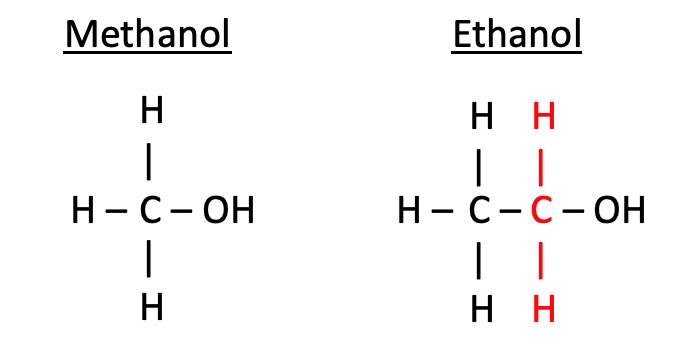
اتانول (C2H5OH): اتانول دارای یک مولکول دو کربنه با فرمول شیمیایی C2H5OH است. معمولاً در مشروبات الکلی یافت می شود و اغلب در زمینه نوشیدنی های الکلی به سادگی به عنوان 'الکل' شناخته می شود.
متانول (CH3OH): متانول یک الکل ساده تر با یک اتم کربن است که با فرمول شیمیایی CH3OH نشان داده می شود. گاهی اوقات الکل چوب نامیده می شود و در درجه اول به عنوان حلال صنعتی و ضد یخ استفاده می شود.
منابع اتانول و متانول:
اتانول: به طور طبیعی از طریق تخمیر قندها توسط مخمر تولید می شود. در نوشیدنی های الکلی مانند آبجو، شراب و الکل یافت می شود.
متانول: می توان آن را از طریق فرآیندهای مختلف، از جمله از گاز طبیعی یا به عنوان محصول فرعی فرآوری چوب، سنتز کرد. همچنین به مقدار کم در برخی از نوشیدنی های الکلی یافت می شود.
موارد استفاده اتانول و متانول
اتانول: کاربردهای وسیعی دارد، از جمله به عنوان نوشیدنی تفریحی، افزودنی سوخت (در بنزین)، حلال در صنایع (داروسازی، آرایشی و بهداشتی و غیره) و به عنوان ضدعفونی کننده و ضد عفونی کننده.
متانول: کاربرد اصلی آن به عنوان حلال صنعتی، ضد یخ و سوخت است. در تولید فرمالدئید و سایر مواد شیمیایی و همچنین در تولید بیودیزل استفاده می شود.
سمیت اتانول و متانول
اتانول: در حالی که مصرف بیش از حد اتانول (الکل) می تواند منجر به مسمومیت و مشکلات سلامتی شود، مصرف متوسط به طور کلی برای اکثر بزرگسالان بی خطر است. بدن می تواند اتانول را در طول زمان متابولیزه کند.
متانول: متانول برای انسان بسیار سمی است و اگر حتی در مقادیر نسبتاً کم مصرف شود، می تواند باعث کوری یا مرگ شود. متانول توسط کبد به فرمالدئید و اسید فرمیک متابولیزه می شود که مسئول اثرات سمی آن هستند.
اثرات بر سلامتی اتانول و متانول
اتانول: به صورت تفریحی در مقادیر متوسط به شکل مشروبات الکلی مصرف می شود. این می تواند اثرات مختلفی بر بدن داشته باشد، از جمله آرامش، کاهش بازداری ها، و اختلال در قضاوت و هماهنگی.
متانول: مصرف متانول می تواند اثرات شدید سلامتی، از جمله اسیدوز متابولیک، آسیب اندام ها، و افسردگی سیستم عصبی مرکزی ایجاد کند. کوری یا مرگ می تواند در اثر مسمومیت با متانول ایجاد شود.
تشخیص اتانول و متانول
اتانول: معمولاً با بو و طعم مشخص آن تشخیص داده می شود. همچنین با استفاده از آزمایش های شیمیایی مختلف به راحتی تشخیص داده می شود.
متانول: متانول از طریق بو و طعم نیز تشخیص داده می شود، اما تشخیص آن از اتانول دشوارتر است. برای شناسایی دقیق متانول از آزمایشهای شیمیایی یا تکنیکهای آزمایشگاهی پیشرفتهتر استفاده میشود.
به طور خلاصه، در حالی که اتانول و متانول هر دو الکل هستند، تفاوت آنها در ساختار شیمیایی، منابع، موارد استفاده، سمیت و اثرات بر سلامت آنها را به موادی متمایز با خواص و کاربردهای منحصر به فرد تبدیل می کند
فرق اتانول و متانول چیست؟
تفاوت در تعداد کربن به کار رفته در ساختار این دو نوع الکل، اصلی ترین فرق اتانول و متانول است. به طور کلی، این دو نوع الکل بسیار شبیه یک دیگر هستند و اکثر اوقات با هم اشتباه گرفته می شوند. اتانول و متانول با وجود شباهت هایی که دارند، دو ماده شیمیایی متفاوت هستند که با یک سری ویژگی های منحصربه فرد هر کدام می شود آنها را از یکدیگر تشخیص داد.
از جمله مواردی که موجب فرق اتانول و متانول می شود، شامل:
در ساختار اتانول حلقه اتیل وجود دارد در حالی که متانول در ساختار خود دارای یک گروه متیل است.
اتانول نسبت به آب اسیدیته ضعیفی دارد در حالی که اسیدیته متانول در مقایسه با آب قوی تر است.
بوی اتانول سنگین و سوزاننده است و شعله این الکل حین سوختن آبی رنگ دیده می شود! در حالی که متانول بوی متفاوتی داشته و شعله آن حین سوختن سفید رنگ است.
اتانول معمولا از روش های طبیعی یعنی تخمیر محصولات غذایی تولید شده ولی متانول معمولا حاصل فرایندهای مصنوعی و صنعتی است.
اتانول خوراکی است! در واقع ماده اصلی نوشیدنی های الکلی را اتانول تشکیل می دهد در حالی که متانول یک ماده سمی بوده و اصلا خوراکی نیست. از متانول برای ساخت فرمالدئید و.. استفاده می کنند.
اتانول چه ویژگی هایی دارد؟
برای درک بهتر فرق اتانول و متانول بهتر است به چند مورد از ویژگی های بارز و منحصر به فرد هر کدام اشاره کنیم.
اتانول را می توان به راحتی در انواع ترکیبات آلی و آب حل کرد! به همین منظور از آن در تولید نوشیدنی های الکلی، رنگ، لاک و سوخت استفاده می شود.
اتانول از هیدراتاسیون اتیل به دست آمده و می توان از آن به عنوان یک ماده ضد عفونی کننده در موارد درمانی و بهداشتی استفاده کرد.
اتانول باعث توزیع بهتر رنگ مواد غذایی شده و عطر و طعم غذا را افزایش میدهد! مثلا یکی از طعم دهنده های غذایی محبوب که با استفاده از اتانول تولید می شود، اسانس وانیل است.
متانول چه ویژگی هایی دارد؟
متانول با نام حلال قطبی الکل چوب هم شناخته می شود! از آن جایی که متانول در گذشته با استفاده از تقطیر مخمر چوب تولید شده است، این نام به متانول اطلاق می شود.
متانول عمدتا از طریق فرایندهای مصنوعی مثل هیدروژناسیون مونوکسید کربن تولید می شود.
از متانول به عنوان یک پیش ماده شیمیایی در ساخت فرمالدئید، اسید استیک، متیل ترت بوتیل اتر و… استفاده می شود.
چگونه فرق اتانول و متانول را تشخیص دهیم؟
بوییدن اولین راه برای تشخیص فرق اتانول و متانول است! متانول بوی تند و تیزی دارد که مشام را اذیت میکند در حالی که اتانول چنین بویی ندارد.
سوزاندن راه دیگر تشخیص این دو ماده است! به این صورت که اگر شعله زرد تا آبی رنگ بود؛ یعنی ماده مورد نظر متانول است! در صورتی که شعله سفید بود یعنی ماده مذکور اتانول می باشد.
یکی از روش های مطمئن تر برای تشخیص اتانول از متانول استفاده از سدیم دی کرومات است! ابتدا به میزان 8 میلی لیتر از سدیم دی کرومات را به 4 میلی لیتر اسید سولفوریک اضافه کنید! حالا 10 قطره از این محلول را به یک ظرف که حاوی الکل است، اضافه کرده و آن را چند بار به آرامی تکان دهید! در این مرحله ظرف مورد نظر را در فاصله 8 تا 12 اینچی از مشام خود نگهدارید و با دست هوای ظرف را به سوی بینی خود هدایت کنید! توجه داشته باشید که نباید ظرف را مستقیما بو کنید چون احتمال دارد مسموم شوید! در صورتی که بوی ظرف تند و تیز باشد، یعنی متانول است! و در صورتی که بوی ملایم و میوه ای داشته باشد، یعنی ماده مذکور اتانول است.
ویژگی های اتانول:
اتانول نوعی الکل با اسکلت کربنی متشکل از یک حلقه اتیل است.
از نظر اسیدیته در مقایسه با آب یک اسید ضعیف است.
بوی سنگین و سوزاننده ای دارد و شعله آبی روشن از خود ساطع می کند.
به طور معمول با تخمیر محصولات غذایی از کارخانه ها تهیه می شود.
اتانول ماده اصلی نوشیدنی های الکلی است.
ویژگی های متانول:
از گروه متیل پیوند کربن تشکیل شده است.
اسیدیته متانول بالاتر از مایعات است.
قابل پیش بینی نیست و بوی مشخصی دارد.
هنگام سوزاندن آن شعله سفید روشن ایجاد می کند.
عمدتا توسط فرآیندهای مصنوعی تولید می شود.
از آنجا که متانول بسیار سمی است ، برای استفاده اصلا مناسب نیست. و به طور کلی در صنعت استفاده می شود.
سوالات متداول:
کدام یک بهتر است؟ اتانول یا متانول؟
مقایسه بین کاهش انتشار HC و سوخت های مخلوط نشان میدهد که متانول موثرتر از اتانول است.
کدام یک مضرتر است؟ اتانول یا متانول؟
متانول نسبت به اتانول بسیار سمی تر است! از اتانول در موارد خوراکی استفاده می شود. در حالی که متانول کاملا سمی بوده و چنین قابلیتی ندارد.
چرا می توانیم اتانول را بنوشیم ولی متانول را نه؟
به دلیل سمی بودن متانول! متانول گاهی اوقات به محصولات اتانولی با مصارف صنعتی مانند حلال ها اضافه می شود تا پتانسیل آنها به عنوان نوشیدنی را رد کند.! با افزودن متانول، تولیدکنندگان می توانند از مالیات های مربوط به مشروبات الکلی اجتناب کنند و محصولات خود را با هزینه کمتر به فروش برسانند.
از آنجایی که این مواد دو ترکیب کاملا متفاوت با یکدیگر هستند، خواص فیزیکی و شیمیایی متفاوتی نیز با یکدیگر دارند که در جدول زیر می توانید مشاهده نمایید:
خواص متانول اتانول:
فرمول شیمیایی CH3OH C2H5OH
جرم مولکولی 32.04 g/mol 46.07 g/mol
رنگ مایع بی رنگ مایع بی رنگ
دانسیته در دمای 20 درجه ی سانتی گراد .0.792 g/m³ 0.7893 g/cm3
نقطه ی جوش 64.7 °C 78.37 °C
نقطه ی انجماد -97.6 °C -114.1 °C
تفاوت در ساختار:
اتانول در ساختار خود دارای گروه اتیل می باشد در حالی که متانول در ساختار خود دارای گروه متیل است.
تفاوت در روش تولید اتانول و متانول:
این دو ماده از نظر روش های تولید هم با یکدیگر کاملا متفاوت هستند. اتیل الکل روش های گوناگونی برای تولید دارد اما عمده ترین روش تولید آن تقطیر مواد حاوی نشاسته نظیر سیب زمینی، نیشکر و ذرت می باشد در حالی که متیل الکل از تقطیر چوب حاصل می گردد.
پیشرفت های فناوری در دهه 1920 و دهه 1970 روند تولید متانول را تغییر داد ، امروزه از گاز طبیعی به عنوان خوراک برای تولید این ماده استفاده می شود. گاز طبیعی از طریق چندین مرحله از جمله استفاده از کاتالیزور ها ، فشار و گرمای زیاد فرآوری می شود و در نهایت به متیل الکل تبدیل می گردد.
تشخیص اتانول طبی و اتانول صنعتی:
نکته:باید توجه نمود که الکل صنعتی می تواند به متانول خالص و یا اتانول صنعتی حاوی متانول اشاره داشته باشد.
نکته: اتانول هم به صورت طبی و هم به صورت صنعتی (حاوی متانول و سمی) در بازار عرضه می گردد.
ممکن است نوشیدنی ها و مواد ضد عفونی کننده حاوی اتانولی که مصرف می کنید در صورتی که از منابع معتبری تهیه نشود حاوی ناخالصی سمی متانول باشد .
الکل صنعتی به دلیل مشمول نشدن در دامنه ی مواد غذایی یا دارویی مالیات کمتری دارد و ارزان تر است و دسترسی به آن راحت تر می باشد.
معمولا تولید کنندگان اتانول صنعتی به دلیل عدم نوشیدن این الکل ها توسط مصرف کنندگان(به دلیل دارا بودن متانول) به آن ترکیبات رنگی اضافه می نمایند و آن را زرد یا نارنجی رنگ می نمایند. باید توجه نمود که برخی افراد سودجو با افزودن آب ژاول (وایتکس) و یا سایر محلول های ضدعفونی کننده و شوینده به اتانول صنعتی آن را به رنگ سفید تبدیل می کنند و به عنوان الکل طبی به فروش می رسانند.
در شکل زیر می توانید تغییر رنگ محلول زرد رنگ الکل صنعتی اتانول را بعد از افزودن محلول پاک کننده ی چند منظوره به سفید و ایجاد رسوب در انتهای ظرف مشاهده نمایید.
راه های شیمیایی تشخیص متانول و اتانول از یکدیگر
یکی دیگر از روش های تشخیص متانول از اتانول مربوط به دمایی است که این ترکیبات به جوش می آیند. نقطه ی جوش متانول خالص 64.7 درجه سانتی گراد (148.5 درجه فارنهایت) است درحالیکه نقطه ی جوش اتانول خالص 78.4 درجه سانتی گراد 173.1 درجه فارنهایت است.”
تشخیص بو:
برای تشخیص این کار 8 میلی لیتر از سدیم دی کرومات و 4 میلی لیتر سولفوریک اسید را با هم مخلوط کنید. سپس 10 قطره از این محلول را با الکل موجود درون لوله ی آزمایش مخلوط کنید. سپس مخلوط را بو نمایید اگر تند و تحریک کننده باشد ، متانول در الکل وجود دارد. اگر رایحه غالب میوه ای باشد ، فقط اتانول موجود است .
رنگ شعله:
رنگ شعله ی نوع خالص اتانول مرکز آبی و در انتها و کناره های شعله زرد رنگ می باشد و متانول خالص کاملا آبی رنگ است.
در ویدیوی زیر نیز می توانید این تفاوت رنگ را مشاهده کنید:
در سوختن هر دوی این ترکیبات در ابتدا هر دو آبی می سوزند اما بعد از مدتی شعله ی اتانول در کناره ها و انتهای شعله زرد رنگ می سوزد(ظرف سمت راست) ولی متانول (ظرف سمت چپ) همچنان آبی خواهد سوخت.
راه های فیزیکی ای مانند بو ، رنگ و تفاوت رنگ شعله در سوختن برای تشخیص این دو ماده از یکدیگر وجود دارد.
اما این روش ها صد درصد قابل اطمینان نیستند و برای تشخیص این دو ماده معمولا از روش های شیمیایی کمک می گیرند
با این که این دو ماده از نظر خواص اندکی با هم تفاوت دارند اما سمیت یکی از این دو باعث شده تا تشخیص دو ماده ی فوق از یکدیگر اهمیت بالایی پیدا نماید.
برای این منظور از تست یدوفرم استفاده می نمایند. اگر دو محلول دارید که نمی دانید کدام متانول (متیل الکل) و یا کدام اتانول (اتیل الکل) است لازم است این تست را انجام دهید.
روش کار:
10 قطره از اتانول و 10 قطره از متانول را در دو ظرف جدا بریزید.
سپس 25 قطره از معرف یداین به هر دو ظرف اضافه کنید
10 قطره از سدیم هیدروکسید به هر دو محلول اضافه نمایید.
سپس محلول ها را هم بزنید تا رنگ تیره ی ید از بین برود و آن را حرارت دهید.
نتیجه:
در طی این آزمایش، با گرم نمودن ظرف حاوی اتیل الکل در حضور سدیم هیدروکسید و یداین رسوب زرد رنگی شکل می گیرد در حالی که این اتفاق برای ظرف حاوی متیل الکل رخ نمی دهد و به واکنش یدوفرم پاسخ مثبت نمی دهد.
CH3CH2OH+I2->CHI3+HCOO–Na
CHI3 رسوب زرد رنگ می باشد.










نظرات کاربران