متانول چیست
متانول که با نامهای متیل الکل یا الکل چوب نیز شناخته میشود، مایعی بیرنگ و فرار است که در صنایع مختلف و زمینه علمی اهمیت زیادی دارد. این یکی از سادهترین الکلها است که از یک اتم کربن منفرد تشکیل شده است

متانول که با نامهای متیل الکل یا الکل چوب نیز شناخته میشود، مایعی بیرنگ و فرار است که در صنایع مختلف و زمینه علمی اهمیت زیادی دارد. این یکی از سادهترین الکلها است که از یک اتم کربن منفرد تشکیل شده است که به سه اتم هیدروژن و یک گروه هیدروکسیل (OH-)پیوند دارد. هدف این مقاله بررسی خواص، روشهای تولید، کاربردها و اثرات بالقوه زیست محیطی متانول است.
متانول یا الکل چوب که سادهترین نوع الکلها است با فرمول شیمیاییCH3OH شناخته میشود.
متانول از فعالیت بیهوازی گونههای زیادی از باکتریها تولید میشود و درنتیجه مقدار اندکی از بخار متانول وارد جو میشود و پس از چندین روز به وسیله اکسیژن و با کمک نور خورشید اکسید شده به آب و دیاکسید کربن تبدیل می گردد. متانول را می توان از منابع طبیعی (مانند انتشار از گیاهان خاص، به عنوان محصول جانبی تجزیه مواد آلی) و همچنین از استفاده انسان از متانول به عنوان یک حلال آزاد کرد. متانول فشار بخار کمی دارد و در هوا تبخیر میشود. با تبخیر شدن در هوا، متانول از طریق واکنش با رادیکالهای هیدروکسیل موجود در هوا تجزیه میشود و نیمه عمری در حدود 18 روز دارد. متانول را میتوان از طریق بارندگی از هوا حذف کرد. در صورت رها شدن در آب، تجزیه متانول از طریق تجزیه زیستی اتفاق میافتد. در صورت رهاسازی متانول در خاک، انتظار میرود متانول تجزیه شده و مستعد شستشو باشد. به دلیل فشار بخار کم متانول، تبخیر سریع از سطوح خشک رخ میدهد.
در ضمن شعله سوختن متانول بیرنگ است و باید مراقب بود تا شعله آن سبب سوختگی نشود. با این حال متانول به مراتب سمیتر از اتانول است. با تولید بیش از ۲۰ میلیون تن در سال، از آن به عنوان پیش ماده دیگر مواد شیمیایی از جمله فرمالدئید، اسید استیک، متیل ترت بوتیل اترژل آتشزا و همچنین میزبان مواد شیمیایی تخصصیتر استفاده میشود.
تاریخچه متانول:
مصریان باستان در فرآیند مومیایی کردن خود از مخلوطی از مواد ازجمله متانول استفاده میکردند که آن را از تجزیه در اثر حرارت چوب به دست میآورند. با این حال، متانول خالص برای اولین بار در سال 1661 توسط رابرت بویل جدا شد، زمانی که او آن را از طریق تقطیر بوکسوس (شمشاد) تولید کرد.بعدها به "روح پیروکسیلیک" معروف شد. در سال ،1834 شیمیدانان فرانسوی ژان باپتیست دوما و یوژن پلیگو ترکیب عنصری آن را تعیین کردند. آنها همچنین کلمه "methylene "را به methy" = مایع الکلی + hȳlē" = جنگل، چوب، الوار مواد تشکیل دادند. "متیلن" یک "رادیکال" را تعیین کرد که حدود 14 درصد وزنی هیدروژن و حاوی یک اتم کربن بود.
شیمیدان فرانسوی پل ساباتیه اولین فرآیندی را ارائه کرد که میتوان از آن برای تولید متانول به صورت مصنوعی در سال 1905 استفاده کرد. این فرآیند نشان داد که دیاکسید کربن و هیدروژن میتوانند برای تولید متانول واکنش نشان دهند. شیمیدانان آلمانی آلوین میتاش و ماتیاس پیر که برای (BASF ) کار میکردند، وسیله ای را برای تبدیل گاز سنتز (مخلوطی از مونوکسید کربن، دیاکسید کربن و هیدروژن) به متانول توسعه دادند و حق ثبت اختراع دریافت کردند.

خواص و تولید متانول:
متانول دارای چندین ویژگی قابل توجه است که به تطبیق پذیری آن کمک میکند. نقطه جوش تقریباً 64.7 درجه سانتیگراد و چگالی ۰.7918 ³cm/g در ۲۰ درجه سانتیگراد است. فرمول شیمیایی آن، CH3OH، ترکیب آن را برجسته میکند، که از یک اتم کربن، چهار اتم هیدروژن و یک اتم اکسیژن تشکیل شده است.
به طور سنتی، متانول با تقطیر مخرب چوب تولید میشد، از اینرو الکل چوب نامیده میشد. با این حال، اکثریت تولید متانول امروزه بر واکنش کاتالیزوری مونوکسید کربن و هیدروژن متکی است که به فرآیند گاز سنتز معروف است. این فرآیند از گاز طبیعی، زغال سنگ یا زیست توده به عنوان ماده اولیه استفاده میکند و متانول را به یک حامل انرژی تجدیدپذیر و همه کاره تبدیل میکند. تولید متانول:
از کاتالیزورهایی که توانایی کار در دماهای پایین مانند مس را دارند، برای تولید موثر متانول استفاده میشود. متانول کم فشار در اواخر دهه 1960 با فناوری متعلق به جانسون متی، ساخته شد. گاز طبیعی اقتصادیترین و پرکاربردترین ماده اولیه برای تولید متانول است. با این حال، از مواد اولیه دیگر نیز میتوان استفاده کرد. از زغال سنگ به عنوان ماده اولیه تولید متانول، به ویژه در چین، استفاده میکنند. علاوه بر این، فنآوریهای بالغ موجود برای گاز دهی زیست توده برای تولید متانول در حال اجرا است. متانول قبالًا توسط تقطیر مخرب چوب تولید میشد. روش مدرن تهیه متانول بر اساس ترکیب مستقیم گاز مونوکسیدکربن و هیدروژن در حضور کاتالیزور است. به طور فزایندهای، سینگاس، مخلوطی از هیدروژن و مونوکسید کربن حاصل از زیست توده، برای تولید متانول استفاده میشود. در واقع به طور کلی تولید متانول شامل هفت مرحله میباشد:
.1 آماده سازی خوراک
.۲ تولید گاز سنتز
.۳ تراکم گاز سنتز شده
.4 سنتز متانول
.5 تصفیه متانول
.6 سیستم بخار و کندانس
.7 ذخیرهسازی و بارگیری
کاربرد متانول:
از مشتقات متانول برای ساخت تعداد زیادی از ترکیبات استفاده میشود، ازجمله بسیاری از مواد رنگزا، رزینها، داروها و عطرهای مهم مصنوعی. مقادیر زیادی برای مواد رنگی به دی متیالنیلین و برای رزینهای مصنوعی به فرمالدئید تبدیل میشود. متانول برای سوخت موتورهای احتراق داخلی بهصورت محدود استفاده میشود، اساساً به این دلیل که تقریباً به اندازه بنزین قابل اشتعال نیست. اشتعال متانول دشوارتر از بنزین است و فقط یک هشتم گرما تولید میکند.
در برخی از تصفیه خانههای فاضلاب، مقدار کمی متانول به فاضلاب اضافه میشود تا منبع غذایی کربن برای باکتریهای ضدعفونی کننده فراهم شود، که نیتراتها را به نیتروژن تبدیل میکنند تا از صاف کننده سفرههای زیرزمینی حساس کاهش یابد.
از متانول به عنوان یک حلال و به عنوان ضدیخ در خطوط لوله و مایع لباسشویی شیشه جلو استفاده میشود. در اوایل دهه ،1900 از متانول به عنوان ضدیخ خنک کننده اتومبیل استفاده میشد. همچنین متانول یک عامل دناتوراسیون در الکتروفورز ژل پلی آکریل آمید است که میتوان در تولید ژل آتشزا استفاده کرد.
هنگام تولید از چوب یا سایر مواد آلی، متانول آلی (الکل زیستی) حاصل به عنوان جایگزین تجدیدپذیر برای هیدروکربنهای پایه نفتی پیشنهاد شده است. با استفاده از مواد حل کننده مناسب و بازدارندههای خوردگی میتوان از سطح پایین متانول در وسایل نقلیه موجود استفاده کرد. دستورالعمل کیفیت سوخت در اروپا اجازه میدهد تا ۳ درصد متانول با مقدار مساوی مواد حلال در بنزین فروخته شده در اروپا مخلوط شود. امروزه چین بیش از یک میلیارد گالن متانول در سال را به عنوان سوخت حمل ونقل در هر دو مخلوط سطح پایین در وسایل نقلیه موجود و هم به عنوان مخلوطهای سطح بالا در وسایل نقلیه طراحی شده برای استفاده از سوختهای متانول استفاده میکند.
پیلهای سوختی متانول مستقیم در دمای پایین و عملکرد فشار جو منحصربه فرد هستند و به آنها اجازه میدهند تا اندازهای بیسابقه کوچک شوند. این ترکیب با ذخیره سازی و جابجایی نسبتاً آسان و بیخطر متانول، ممکن است امکان الکترونیکی مصرفی مجهز به سلول سوختی، مانند رایانههای لپتاپ و تلفنهای همراه را فراهم کند.
متانول همچنین به عنوان سوخت در اجاقهای کمپینگ و قایقرانی بسیار استفاده میشود. متانول در مشعلهای تحت فشار خوب میسوزد. اجاقهای الکلی معمولا کمی بیشتر از یک فنجان برای نگهداری سوخت نیاز دارند. این عدم پیچیدگی باعث میشود که مسافران بیشتر وقت خود را در بیابان بگذرانند یا به عنوان مواد اولیه اصلی در تولید gel (ژل آتشزا) استفاده میشود(starter fule).
متانول یک حلال رایج آزمایشگاهی است. به دلیل قطع کم اشعه ماورا بنفش، به ویژه برای طیف سنجیHPLC کروماتوگرافی مایع با کارایی بالا و VIS / UV بسیار مفید است.
تاکنون بیشترین کاربرد متانول در ساخت سایر مواد شیمیایی است. تقریباً 40 درصد متانول به فرمالدئید تبدیل میشود. سپس برای ساخت سایر محصولات به تنوع پلاستیک، تخته سه ال، رنگ، مواد منفجره و منسوجات پرس دائمی مورد استفاده قرار میگیرد.
سایر مشتقات شیمیایی متانول شامل دی متیل اتر است که جایگزین کلروفلوئورکربنها بهعنوان یک ماده محرک اسپری آئروسل و اسید استیک شده است. دی متیل اتر یا“DME “همچنین میتواند با گاز مایع (LPG) برای گرم کردن و پخت وپز در خانه مخلوط شود، و میتواند به عنوان سوخت حمل ونقل جایگزین دیزل استفاده شود.
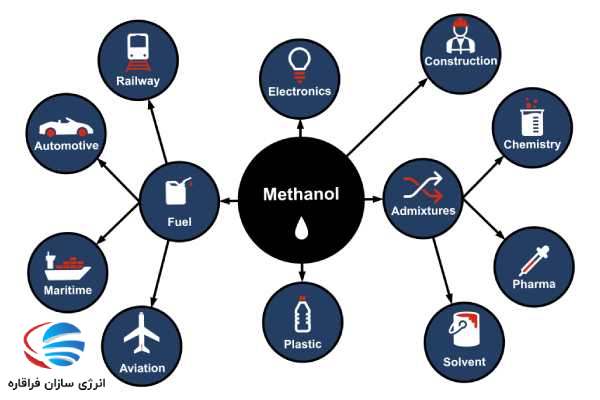
کاربرد متانول در صنعت:
متانول به دلیل خواص منحصربه فردش، کاربرد گسترده ای در صنایع مختلف پیدا میکنند. یکی از کاربردهای برجسته آن به عنوان ماده اولیه در تولید مواد شیمیایی مانند فرمالدئید، اسید استیک و متیل تری بوتیل اتر (MTBE) است. فرمالدئید، مشتق شده از متانول، به عنوان یک ماده خام حیاتی برای ساخت رزین، پالستیک و منسوجات عمل میکند. علاوه بر این، خواص حلال متانول آن را برای استفاده به عنوان یک عامل تمیزکننده، افزودنی سوخت و جزء ضد یخ مناسب میکند. علاوه بر این، متانول به عنوان یک منبع سوخت جایگزین شناخته شده است. میتوان از آن به عنوان جایگزینی برای بنزین در وسایل نقلیه استفاده کرد و احتراق تمیزتر و کاهش انتشار گازهای گلخانهای را فراهم کرد. سلولهای سوختی متانول نیز به عنوان یک منبع انرژی بالقوه برای وسایل نقلیه الکتریکی مورد بررسی قرار میگیرند، زیرا آنها چگالی انرژی بالا و قابلیت سوختگیری سریع را ارائه میدهند.
متانول به عنوان ضدیخ، حلال و سوخت بکار برده میشود. از متانول برای تقلیب اتانول نیز استفاده میشود، این عمل به منظور غیرقابل شرب نمودن اتانولی که برای مصارف صنعتی تولید میشود انجام میپذیرد (در کشورهای اسلامی به جهت مسائل شرعی و در کشورهای دیگر به جهت معافیت از مالیات فروش مواد مست کننده) بدین منظور از مواد دیگری چون پریدین و تربانتین نیز استفاده میشود.
متانول به صورت محدود به عنوان سوخت در موتورهایی با سیستم احتراق داخلی استفاده میشود. متانول تولید شده از چوب و سایر ترکیبات آلی را متانول آلی یا بیو الکل مینامند که یک منبع تجدید شدنی برای سوخت است و میتواند جایگزین مشتقات نفت خام شود. با این همه، از بیو الکل 100 درصد نمیتوان در ماشینهای دیزلی بدون ایجاد تغییر در موتور ماشین .استفاده کرد. متانول به عنوان حلال ضدیخ و در تهیه سایر ترکیبات شیمیایی استفاده میشود
4۰ درصد از متانول تولیدی برای تهیه فرمالدئید استفاده میشود که آن هم در تهیه پلاستیک، تخته، رنگ و مواد منفجره استفاده میشود. برای تغییر ماهیت اتانول صنعتی و جلوگیری از کاربرد آن به عنوان نوشیدنی، مقداری متانول به آن اضافه میکنند. دی متیل اتر از مشتقات متانول است که به جای CFC ها در افشانههای آتروسل به عنوان پیشرانه استفاده میشود.
همچنین از متانول در تهیه استیک اسید و متیل ترشیو بوتیل اتر نیز استفاده میشود.
استفاده از متانول به عنوان سوخت:
یکی از اشکالات متانول به عنوان سوخت، خوردگی آن در برخی فلزات ازجمله آلومینیوم است. متانول، اگرچه اسید ضعیفی است، اما به پوشش اکسیدی حمله میکند که به طور معمول آلومینیوم را از خوردگی محافظت میکند:
CH3OH + Al2O3 → 2Al (OCH3)3 + 3H2O6
نمکهای متوکسید حاصل در متانول محلول هستند و درنتیجه سطح آلومینیوم تمیز ایجاد میشود که بهراحتی توسط مقداری اکسیژن محلول اکسید میشود. همچنین متانول میتواند به عنوان یک اکسید کننده عمل کند:
CH3OH + 2Al → 2Al (OCH3)3 + 3H2O6
این فرآیند متقابل تا زمانی که فلز از بین نرود یا غلظت CH3OH ناچیز باشد، به طور مؤثر سوختگی را تقویت میکند. با استفاده از مواد سازگار با متانول و مواد افزودنی سوختی که به عنوان بازدارنده های خوردگی عمل میکنند. نگرانیهای مربوط به خوردگی متانول رفع شده است. مسمومیت متانول:
در انسان، متانول سمیت بالایی دارد. متانول با دو مکانیسم سمی است. اول، متانول، چه بلعیده شود، چه استنشاق شود و چه از طریق پوست جذب شود، به دلیل خواص مهارکننده CNS مانند روش مسمومیت با اتانول میتواند کشنده باشد. دوم، در یک فرآیند مسمومیت، جایی که از طریق فرمالدئید در فرآیندی که توسط آنزیم الکل دهیدروژناز در کبد آغاز میشود، به اسید فرمیک متابولیزه میشود. واکنش برای تشکیل بهطور کامل ادامه مییابد و هیچ فرمالدئید قابل تشخیصی باقی نمیماند. مسمومیت با متانول را میتوان با پادزهرهای اتانول یا فومپیزول درمان کرد. هردوی این داروها برای کاهش عملکرد الکل دهیدروژناز بر روی متانول از طریق مهار رقابتی عمل میکنند بنابراین بیشتر از اینکه به متابولیت های سمی تبدیل شود، از طریق کلیه ها دفع میشود. علائم اولیه مسمومیت با متانول شامل افسردگی سیستم عصبی مرکزی، سردرد، سرگیجه، حالت تهوع، عدم هماهنگی، گیجی و با دوزهای کافی زیاد، بیهوشی و مرگ است. علائم اولیه قرار گرفتن در معرض متانول معمولًا کمتر از علائم ناشی از بلع مقدار مشابهی از اتانول است. هنگامی که علائم اولیه از بین رفت، دسته دیگری از علائم، 10 تا 30 ساعت پس از قرار گرفتن در معرض اولیه متانول، شامل تاری یا از بین رفتن کامل بینایی و اسیدوز، ظاهر میشوند. این علائم درنتیجه تجمع سطح سمی فرمات در جریان خون است و ممکن است در اثر نارسایی تنفسی تا حد مرگ پیشرفت کند. مشتقات استر متانول این سمیت را ندارند. هنگام استفاده از متانول باید از ماسک و دستکش استفاده کرد چون از طریق تنفس و پوست و آشامیدن نیز میتواند جذب شود.

نکاتی که در مصرف الکل صنعتی باید رعایت نمود:
1-الکل صنعتی به طور معمول در رنگ های زرد یا آبی عرضه میشود
2-الکل صنعتی پایه متانول بوده و سمی است
3-الکل متانول به صورت بیرنگ بوده و برای تشخیص الکل صنعتی با الکل طبی به آن رنگ اضافه شده که مصرف کننده را به سمی بودن آن آگاه سازد.
4-الکل صنعتی در بطریهای پت یا پلاستیکی عرضه میشود
5-الکل صنعتی برای مصرف بهداشتی و خوراکی نمیباشد
6-از الکل صنعتی (متانول) برای مصارف زیر استفاده میشود:
الف -جرم گیری و لکه گیری اماکن ،سطوح، کاشی، سرامیک، و قطعات و قالبهای فلزی استفاده میشود
ب- سوخت چراغهای الکلی، آزمایشگاهی، مشتعل کننده ذغال و چوب
ج– حلال چربیها و جرم گیری و جهت نظافت و جرم گیری قطعات ابزار و لوازم الکتریکی کامپیوتر و ماشینآلات
د- جلاه دهنده و درخشان کننده سطوح
ه- پاک کننده دوده و چربی
7- در جای خنک و دور از دسترس اطفال نگهداری شود
8- از تماس با پوست جدا خودداری گردد
9- جهت استفاده از دستکش استفاده شود
10- هنگام خریدن الکل صنعتی دقت نمایید که دارای لیبل با مشخصات دقیق شامل آدرس کارخانه یا دفتر مرکزی شماره تلفن .پروانه بهره برداری بارکد خوانا جهت استفاده دستگاههای فروشگاهی بارکدخوان باشد
11- بر روی لیبل موارد مصرف قید شده باشد
12 علائم ایمنی (خطرناک بودن و سمی بودن) به وضوح و خوانا قید شده باشد
13 - درب بطری را بعد ازمصرف محکم ببندید که از تبخیر جلوگیری گردد
نتیجه:
متانول به عنوان یک ترکیب همه کاره با کاربردهای متنوع در صنایع و زمینههای علمی مختلف عمل میکند. خواص منحصربه فرد آن را برای تولید مواد شیمیایی، جایگزینهای سوخت و تحقیقات علمی مناسب میکند. با این حال، تعادل مزایای آن با ملاحضات زیست محیطی بالقوه با اتخاذ روشهای تولید پایدار و ترویج مدیریت مسئولانه ضروری است. با استفاده از پتانسیل متانول و درعین حال به حداقل رساندن اثرات زیست محیطی آن، می توانیم از این ترکیب به عنوان یک منبع ارزشمند برای آینده ای پایدار استفاده کنیم.









نظرات کاربران